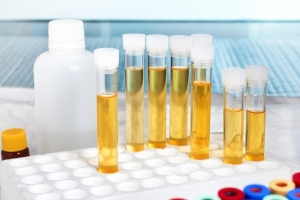
HEMOCULTIVO
Datos requeridos para la solicitud de un hemocultivo
• Nombre y apellido del paciente. Si el paciente no está reconocido entonces se utilizará el nombre de la madre pero debe especificar esta condición con la palabra “hijo”.
• Número de registro o cédula del paciente. Si el paciente no tiene este tipo de identificación se podrá utilizar la cédula de la madre.
• Fecha y hora de solicitud del hemocultivo.
• Fecha y hora de toma del hemocultivo.
• Fecha de nacimiento del paciente.
• Peso del paciente en kilogramos.
• Sitio de toma del hemocultivo (Sangre periférica, línea arterial, catéter venoso central). Anotar en la volante de Laboratorio Clínico el sitio de la toma de la muestra.
• Volumen de sangre inoculado en el hemocultivo en mililitros.
• Número de set de hemocultivo (un set generalmente incluye una botella aeróbica y una anaeróbica). Cada set debe ser identificado como: set # 1 ó set # 2. Y el número de botella correspondiente.
• Nombre del médico que solicita el hemocultivo.
• Nombre del personal que realiza la extracción.
• Anotar en la solicitud si se está utilizando algún antibiótico.
A los pacientes con un peso mayor a 2 Kg. se les debe tomar dos sets de hemocultivos, los cuales deben ser obtenidos de sitios diferentes de extracción en un periodo entre 30 y 90 minutos, excepto en pacientes graves que requieran inicio inmediato de antibióticos, en los cuales se podrán tomar los dos sets de hemocultivos seguidos, sólo cambiando el sitio de punción.
En pacientes con sospecha de bacteriemia intermitente se recomienda tomar múltiples hemocultivos separados por 6 a 36 horas.
La siguiente tabla específica el volumen total de sangre que debe ser recolectado para cada set de hemocultivo, según el peso del paciente.
|
Volúmenes de sangre recomendados para hemocultivos en pacientes pediátricos. |
||||
| Peso del Paciente (kg) |
Volumen de sangre a extraer (ml) |
|||
|
Primera serie |
Segunda serie |
|||
|
Botella aeróbica |
Botella anaeróbica |
Botella aeróbica |
Botella
anaeróbica |
|
| ≤ 1.0 | 1.0 | —— | —— | —— |
| 1.1-2.0 | 2.0 | —— | —– | —— |
| 2.1-3.0 | 2.0 | —— | 2.0 | —— |
| 3.1-12.7 | 4.0 | —— | 2.0 | —— |
| 12.8-36.3 | 5.0 | 5.0 | 5.0 | 5.0 |
| >36.3 | 10 | 10 | 10 | 10 |
| a) La primera botella de cada serie corresponde a la botella aeróbica y la segunda, a la botella anaeróbica. En ausencia de indicación de hemocultivo anaerobio, se colocará todo el volumen correspondiente a esa serie en una botella aeróbica.
b) Los sets de hemocultivos se deben tomar con una diferencia de 30 a 90 min, excepto en pacientes graves que requieren inicio inmediato de antibióticos. En estos últimos, los 2 sets de hemocultivos se pueden tomar seguidos sólo cambiando el sitio de punción. c) En botellas pediátricas se puede inocular un máximo de 4 ml de sangre. Si el volumen requerido es mayor de este volumen, se solicitará una botella para adultos o se utilizarán dos botellas pediátricas. |
||||
Protocolo de flebotomía recomendado para la toma de muestras de hemocultivos
A continuación se describen los pasos necesarios para reducir la tasa de contaminación durante el proceso de recolección de muestras de hemocultivos:
• Solicitar apoyo para realizar el procedimiento. La toma de hemocultivo requiere siempre de la presencia de un asistente.
• Preparar los materiales necesarios.
• Preguntar al paciente, tutor o padres si están de acuerdo con la extracción de muestras para hemocultivo. Informar y tranquilizar al paciente.
• Identificar adecuadamente al paciente por su nombre y apellido, verifique su registro médico o cédula.
• Lavarse las manos con agua y jabón.
• Utilizar guantes desechables limpios.
• Preparar la botella de hemocultivo para la inoculación, retire las tapas sin contaminar y limpie la parte superior con alcohol isopropílico al 70%.
• Evaluar y seleccionar el sitio de punción.
• Limpiar el sitio de punción con alcohol al 70% con un movimiento circular del centro hacia afuera con un diámetro de 5 a 8 cm. Si la gasa o algodón se ven sucios después de la limpieza, utilice una segunda limpieza.
• Para desinfectar el área, utilizar una almohadilla estéril impregnada con gluconato de clorhexidina al 2%, aplicando sobre el área punción desde del centro hacia afuera con movimientos circulares hasta cubrir un área de dos a tres pulgadas de diámetro.
• Repetir el procedimiento con una segunda almohadilla humedecida con el desinfectante. (deje secar por un mínimo de 30 segundos).
• Colocar el torniquete entre 5 y 8 cm del sitio de extracción, siendo cuidadoso de no tocar el área desinfectada con el mismo o con los guantes. Si el torniquete ha permanecido en el sitio por más de 2 minutos, se debe quitar y esperar 2 minutos antes de volver a colocar. Mantener el torniquete más de 2 minutos puede producir hemólisis y alterar los resultados.
• Colocarse guantes estériles
• Ejecutar la flebotomía usando jeringas de tamaño acorde al volumen de sangre que se requiere extraer.
• Cubrir el sitio de punción con una gasa estéril para no contaminar la muestra.
• Inocular primero la botella aeróbica y luego la anaeróbica.
• Inocular la sangre en la botella de hemocultivo con la aguja que utilizó para realizar la extracción.
• Si se está extrayendo sangre para otras pruebas con la misma jeringa, primero debe inocular las botellas de hemocultivo antes de inyectar la sangre en otros tubos/botellas. Realizar la inoculación en otro orden puede contaminar la botella de cultivo e invalidar el resultado del mismo.
• Mezclar la botella suavemente y varias veces para evitar la formación de coágulos.
• Si la botella cuenta con etiqueta de código de barra desprendible, pegarlo en la solicitud.
• Desechar la aguja y jeringa en un contenedor adecuado.
• Enviar la muestra de hemocultivo al laboratorio siguiendo el protocolo estándar de manejo y transporte de hemocultivos.
• Usar alcohol isopropílico al 70% para limpiar el área donde se realizó la extracción de la muestra. (eliminar los restos de gluconato de clorhexidina 2%)
• Retirar los guantes y descártelos en un contenedor apropiado.
• Lavarse las manos al terminar
Recomendaciones
- Para infantes y niños pequeños el volumen de sangre extraído no debe ser mayor del 1% del volumen total del paciente.
- Si se utiliza solamente botellas aeróbicas, se deben utilizar dos botellas en el caso que sea necesario para completar el volumen correspondiente a esa serie.
- La sangre puede ser extraída directamente en contenedores que contengan polyanetholsulfonato de sodio (SPS), pero jamás deberán ser tomados en contenedores con otros anticoagulantes.
- La muestra de sangre para hemocultivo debe extraerse, siempre que sea posible, por punción venosa. La utilización de sangre arterial no ha demostrado ventajas sobre la venosa.
UROCULTIVO
Los especímenes de orina pueden ser contaminadas con flora perianal, periuretral o vaginal durante la recolección.
La técnica de recolección de muestras de orinas es crítica, desde que una muestra es recolectada de forma inadecuada a menudo resulta en la producción de datos inexactos.
A continuación se muestran los tipos de técnica para la recolección de orina:
VALORES NORMALES HEMATOLOGIA
PRUEBAS Y CONDICIONES PARA LA TOMA DE MUESTRA DE LA SECCIÓN DE HEMATOLOGÍA
| Prueba | CONDICIÓN REQUERIDA DEL PACIENTE | CONTENEDOR Y VOLUMEN DE MUESTRA | CONTENEDOR Y VOLUMEN DE MUESTRA | INTERFERENTES/ LIMITACIONES / FUENTES DE VARIACIÓN | Temperatura | Tiempo | Tipo de Muestra | DIA QUE SE EFECTÚA LA PRUEBA | TIEMPO DE ENTREGA DE RESULTADOS |
|---|---|---|---|---|---|---|---|---|---|
| Hemograma | Ninguna | Microtubo/Tubo de tapa lila 375-500 µl/1-2 ml |
AIM Impedancia Electrónica Observación Microscópica |
No se procesan muestras con coagulo y microcoágulo. | Ambiente 2– 8 °C | 6 horas 24 horas |
Sangre Completa en EDTA | DIARIO | DIARIO |
| Coagulación | Se recomienda ayuno de 2 horas | Microtubo/Tubo de tapa celeste 1 ml/1.8 ml | Densidad Óptica | No se procesan muestras con coagulo y microcoágulo. Hemolísis, ictericia y lipemia. Contenedor con sobre o baja cantidad de muestra. |
Ambiente 2– 4 °C | 2 horas | Plasma en Citrato de Sodio | DIARIO | DIARIO |
| Electroforesis de Hemoglobina |
Ninguna | Microtubo/Tubo de tapa lila 1 ml |
HPLC | Ambiente 2– 8 °C | 2 horas 7 dias |
Sangre Completa en EDTA | LUNES A VIERNES | LUNES A VIERNES | |
| Hemoglobina glicosilada | Ninguna | Microtubo/Tubo de tapa lila 1 ml |
HPLC | Cualquier condición que disminuya la vida media de los eritrocitos disminuye los valores. HbD y HbE HbF >30% |
Ambiente 2– 8 °C | 2 horas 7 dias |
Sangre Completa en EDTA | LUNES A VIERNES | LUNES A VIERNES |
Valores Normales de Referencia Hemograma
| edad | WBC
x 103/ul |
RBC
x 106/ul |
HGB
g/dL |
HCT
% |
VCM
FL |
hcm
PG |
PLAQUETAS
103/ul |
RDW
% |
CHCM
g/dl |
vpm
FL |
|---|---|---|---|---|---|---|---|---|---|---|
| Neonatos | 9.1 – 34.3 | 4.1 – 6.7 | 15.0 – 24.0 | 44 – 78 | 102 – 115 | 33 – 39 | 150 – 450 | 13.0 – 18.0 | 32 – 36 | 6.0 – 9.5 |
| 29 días – 23 meses | 6.0 – 14.0 | 3.8 – 5.4 | 10.5 – 14.0 | 32 – 42 | 72 – 88 | 24 – 30 | 150 – 450 | 11.5 – 16.0 | 32 – 36 | 6.0 – 9.5 |
| 2-9 años | 4.0 – 12.0 | 4.0 – 5.3 | 11.5 – 14.5 | 33 – 43 | 76 – 90 | 25 – 31 | 150 – 450 | 11.5 – 15.0 | 32 – 36 | 6.0 – 9.5 |
| 10 – 17 años
Varones Mujeres |
4.0 – 10.5
4.0 – 10.5 |
4.2 – 5.6
4.1 – 5.3 |
12.5 – 14.1
12.0 – 15.0 |
36 – 47
35 – 45 |
80 – 95
80 – 95 |
27 – 32
27 – 32 |
150 – 450
150 – 450 |
11.5 – 14.5
11.5 – 14.5 |
32 – 36
32 – 36 |
6.0 – 9.5
6.0 – 9.5 |
| >18 años
Varones Mujeres |
4.0 – 10.5
4.0 – 10.5 |
4.7 – 6.0
4.2 – 5.4 |
13.5 – 18.0
12.5 – 16.0 |
42 – 52
37 -47 |
80 – 100
80 – 100 |
27 – 32
27 – 32 |
150 – 450
150 – 450 |
11.5 – 14.5
11.5 – 14.5 |
32 – 36
32 – 36 |
6.0 – 9.5
6.0 – 9.5 |
Valores Normales de Referencia Diferencial Leucocitario en Porcentaje
| Edad | Neutrófilos Segmentados % | Neutrófilos Banda % | Linfocitos % | Mononucleares % | Eosinófilos % | Basófilos % |
|---|---|---|---|---|---|---|
| Neonatos | 40 -60 | < 3.5 | 20 – 40 | 1 – 12 | 1 – 6 | 0 – 2 |
| 29 dias – 23 meses | 20 – 40 | < 1 | 50 – 60 | 2 – 11 | 1 – 6 | 0 – 2 |
| 2 – 9 años | 35 – 50 | < 1 | 40 – 60 | 2 – 11 | 1 – 4 | 0 – 2 |
| 10 – 17 años | 35 – 55 | < 1 | 30 – 50 | 2 – 11 | 1 – 3 | 0 – 2 |
| >18 años | 50 – 60 | < 1 | 30 – 50 | 2 – 11 | 1 – 3 | 0 – 2 |
Valores Normales de Referencia Diferencial Leucocitario Valor Absoluto
| edad | Neutrófilos Totales † x 103/ul‡ |
Neutrófilos Segmentados x 103/ul‡ |
Neutrófilos Banda x 103/ul‡ |
Linfocitos x 103/ul ‡ | Mononucleares x 103/ul ‡ | Eosinófilos x 103/ul ‡ |
Basófilos 103/ul ‡ |
|---|---|---|---|---|---|---|---|
| Neonatos | 6.0 – 23.5 | 6.0 – 20.0 | ‹ 3.5 | 2.5 – 10.5 | ‹ 3.5 | ‹ 2.0 | ‹ 0.4 |
| 29 dias – 23 meses | 1.1 – 6.6 | 1.0 – 6.0 | ‹ 1.0 | 1.0 – 9.0 | ‹ 1.0 | ‹ 0.7 | ‹ 0.1 |
| 2 – 9 años | 1.4 – 6.6 | 1.2 – 6.0 | ‹ 1.0 | 1.0 – 5.5 | ‹ 1.0 | ‹ 0.7 | ‹ 0.1 |
| 10 – 17 años | 1.5 – 6.6 | 1.3 – 6.0 | ‹ 1.0 | 1.0 – 3.5 | ‹ 1.0 | ‹ 0.7 | ‹ 0.1 |
| >18 años | 1.5 – 6.6 | 1.3 – 6.0 | ‹ 1.0 | 1.5 – 3.5 | ‹ 1.0 | ‹ 0.7 | ‹ 0.1 |
Valores Normales de Referencia de Velocidad de Eritrosedimentación (VES)
| Edad | mm/hora |
|---|---|
| Neonatos | 0 – 2 |
| 29 días – 23 meses | 0 – 10 |
| 2 – 9 años | 0 – 11 |
Valores Normales de Referencia de Electroforesis de Hemoglobina
| Edad | Hgb A1 % |
Hgb A2 %‡ |
Hgb F %‡ |
Hgb S %‡ |
Hgb C %‡ |
|---|---|---|---|---|---|
| Neonatos | 26.5 – 46.5 | < 3.5 | 50 – 80 | 0 | 0 |
| 29 días – 23 meses | 46.5 – 94.5 | < 3.5 | 2 – 50 | 0 | 0 |
| >2 años | 95 | 2.0 – 3.5 | 0.8 – 2.0 | 0 | 0 |
VALORES DE REFERENCIA EN URINÁLISIS Y PARASITOLOGÍA
EXÁMENES DE URINÁLISIS
Intervalos Biológicos de Referencia
| PRUEBA | INTERVALOS DE REFERENCIA | MUESTRA | DÍA EN QUE SE EFECTÚA | INDICACIONES PARA LA PRUEBA | |
| Rango | Unidad | ||||
| EXAMEN MACROSCÓPICO | |||||
| COLOR | Amarillo Claro Amarillo Oscuro |
Orina | Lunes a Domingo | Ninguna | |
| ASPECTO | Claro Ligeramente Turbio |
Orina | Lunes a Domingo | Ninguna | |
| GRAVEDAD ESPECÍFICA | 1.015 – 1.025 >1.025 con restricción de agua |
Orina | Lunes a Domingo | Ninguna | |
| REACCIÓN (pH) | 5.0 – 8.0 | Orina | Lunes a Domingo | Ninguna | |
| ALBÚMINA | Negativa | Orina | Lunes a Domingo | Ninguna | |
| GLUCOSA | Negativa | Orina | Lunes a Domingo | Ninguna | |
| ACETONA | Negativa | Orina | Lunes a Domingo | Ninguna | |
| BILIS | Negativa | Orina | Lunes a Domingo | Ninguna | |
| SANGRE OCULTA | Negativa | Orina | Lunes a Domingo | Ninguna | |
| NITRITO | Negativo | Orina | Lunes a Domingo | Ninguna | |
| UROBILINÓGENO | Normal ó 0.2 – 1 | mg/dl | Orina | Lunes a Domingo | Ninguna |
| BACTERIAS | No se observó | Orina | Lunes a Domingo | Ninguna | |
| ERITROCITOS | 0 – 3 XC | Orina | Lunes a Domingo | Ninguna | |
| MUCOSIDADES | No se observó | Orina | Lunes a Domingo | Ninguna | |
| TRICOMONAS | No se observó | Orina | Lunes a Domingo | Ninguna | |
| LEVADURAS | No se observó | Orina | Lunes a Domingo | Ninguna | |
| CRISTALES | No se observó | Orina | Lunes a Domingo | Ninguna | |
| CILINDROS | No se observó | Orina | Lunes a Domingo | Ninguna | |
| PRUEBAS CONFIRMATORIAS | |||||
| ALBÚMINA (Ácido Sulfosalicílico al 3%) |
Negativa Positiva | Trazas 1+ 2+ 3+ 4+ |
Orina | Lunes a Domingo | Ninguna |
| GLUCOSA | Negativa Positiva |
Orina | Lunes a Domingo | Ninguna | |
| ACETONA | Negativa Positiva |
Orina | Lunes a Domingo | Ninguna | |
| BILIRRUBINA | Negativa Positiva |
Orina | Lunes a Domingo | Ninguna | |
| UROBILINÓGENO | Negativa Positiva |
Orina | Lunes a Domingo | Ninguna | |
EXÁMENES DE PARASITOLOGÍA
Intervalos Biológicos de Referencia
| PRUEBA | INTERVALOS DE REFERENCIA | MUESTRA | DÍA EN QUE SE EFECTÚA | INDICACIONES PARA LA PRUEBA |
| Rango Unidad | ||||
| HECES GENERALES | ||||
| COLOR | Chocolate | Heces | Lunes a Domingo | Ninguna |
| APARIENCIA | Formada a Pastosa | Heces | Lunes a Domingo | Ninguna |
| AMEBAS | No se observó | Heces | Lunes a Domingo | Ninguna |
| PARÁSITOS | No se observó | Heces | Lunes a Domingo | Ninguna |
| OTROS EXÁMENES | ||||
| SANGRE OCULTA | Negativa | Heces | Lunes a Domingo | Ninguna |
| LEUCOCITOS | No se observó 0 % 0 % |
Heces | Lunes a Domingo | Ninguna |
| (Azul de Metileno) | ||||
| Polimorfonucleares | ||||
| Mononucleares | ||||
| pH | 6.5 – 7.5 | Heces | Lunes a Domingo | Ninguna |
| Grasas | No se observó | Heces | Lunes a Domingo | Ninguna |
| Rotavirus | Negativo | Heces | Lunes a Domingo | Ninguna |
| APT | Hemoglobina Materna (Negativo) Hemoglobina Fetal (Positivo) | Sangre emitida por: Ano/Heces Aspirado Gástrico Vómito |
Lunes a Domingo | Ninguna |
REQUISITOS PARA ENVIO DE MUESTRAS AL LABORATORIO CLÍNICO
Laboratorio Clínico del Hospital del Niño Dr. José Renán Esquivel
Requisitos para el envío de muestras al laboratorio.
| Prueba | Muestra | Formulario | Temperatura | Prueba |
| Tosferina | Hisopado Nasofaríngeo (2 hisopados) | Formulario de notificación Obligatoria y Formulario de investigación de tosferina | En frío 4-8ºC | RT-PCR |
| Zika, Dengue, Chikungunya | Tubo de química lleno | Formulario de notificación Obligatoria y Formulario de Dengue | En frío 4-8ºC | RT-PCR |
| C. trachomatis, M. genitalis, | Hisopo | Formulario de notificación Obligatoria | En frío 4-8ºC | RT-PCR |
| N. gonorrhoeae, U. urealytycum |
Orina | |||
| T. vaginalis, M. hominis, | Hisopo, Orina | Formulario de notificación Obligatoria | En frío 4-8ºC | RT-PCR |
| Herpes simplex 1 y 2 | LCR, sangre venosa. Tomada en tubo con EDTA 2mL | |||
| Citomegalovirus | Sangre venosa. Tomada en tubo con EDTA 2mL | Formulario de notificación Obligatoria | En frío 4-8ºC | RT-PCR |
| Ebstein-Barr virus | Sangre venosa. Tomada en tubo con EDTA 2mL | Formulario de notificación Obligatoria | En frío 4-8ºC | RT-PCR |
| HIV carga viral | Sangre venosa. Tomada en tubo con EDTA 2mL | Formulario de notificación Obligatoria | En frío 4-8ºC | RT-PCR |
| Mycobacterium tuberculosis Enterovirus |
Esputo, LBA, Tejido fresco, orina Líquido Cefalorraquídeo |
Formulario de Notificación Micobacteriología Formulario de notificación Obligatoria |
TA 20-25ºC En frío 4-8ºC |
RT-PCR RT-PCR |
| Clostridium difficile | Heces diarréicas | Formulario de notificación Obligatoria | En frío 4-8ºC | RT-PCR |
| Virus Sincicial Respiratorio | Hisopado Nasofaríngeo Lavado/aspirado nasales | Formulario de notificación Obligatoria F. vigilancia Neumonía y Bronquiolitis |
2-30ºC | RT-PCR |
| Influenza A y B VRS, Rinovirus, Parainfluenza, Metapneumovirus, Adenovirus) |
Hisopado Nasofaríngeo Lavado/aspirado nasales Hisopado Nasofaríngeo |
Formulario de notificación Obligatoria Formulario de vigilancia Neumonía y Bronquiolitis |
2-30ºC | RT-PCR |
| Histoplasma capsulatum | Sangre venosa. Tomada en tubo con EDTA 2mL | Formulario de notificación Obligatoria. | 2-30ºC | PCR |
| Encefalitis Equina (EEV y EEE) | LCR y SUERO | Formulario de notificación Obligatoria. Formulario de Encefalitis |
En frío 4-8ºC | Mac ELISA IgM/ELISA Ig G |
TÉCNICAS Y QUÍAS PARA LA RELOCECCIÓN DE MUESTRAS 2019